Atomic structure : परमाणु संरचना
Science : Atomic structure
परमाणु संरचना
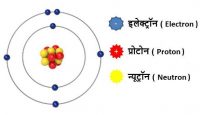
इलेक्ट्रॉन ( Electron )
सन 1897 में सर विलियम क्रुक ने ज्ञात किया कि विसर्जन नलिका में बहुत कम दाब पर भरी गैस में इलेक्ट्रॉनों पर उच्च विद्युत वोल्टता प्रयुक्त करने से कैथोड किरणें निकलती हैं इन किरणों की प्रकृति ऋण आत्मक होती है
सन 1897 में सर जे जे थॉमसन ने विद्युत और चुंबकीय क्षेत्रों के द्वारा कैथोड किरणों के विक्षेप का अध्ययन करके निष्कर्ष निकाला कि कैथोड किरणों में ऋण आवेशित कण होते हैं इलेक्ट्रॉन की खोज का श्रेय सर जेजे थॉमसन को है सन 1990 आर ए मिलीकन ने इलेक्ट्रॉन पर आवेश ज्ञात किया
e=4.8× 10 की पावर - 10 esu या 1.6 * 10 की पावर - 19 होता है
इलेक्ट्रॉन का द्रव्यमान = 9.11 * 10 की पावर - 28
प्रोटोन ( Proton )
सर जेजे थॉमसन ने सिद्ध किया किरणों के धन आवेश कण होते हैं इनको धन किरण या कैनल किरण नाम दिया गया प्रोटोन की खोज का श्रेय गोल्डस्टीन को जाता है जबकि नाभिक की खोज का श्रेय रदरफोर्ड को जाता है
न्यूट्रॉन ( Neutron )
सन 1930 में बोथे और बेकर ने कुछ हल्के तत्वों को अल्फा कणों द्वारा बमबारी करके बहुत अंतर्वेदी विकिरणों को ज्ञात किया सन 1932 में चैडविक ने बताया कि इन विकिरण में निश्चय ही उदासीन कण होते हैं जिसे हम न्यूट्रॉन कहते हैं प्रोटॉन और न्यूट्रॉन की द्रव्यमान समान होते हैं जो कि
1.00 732 एएमयू or 1.67 25 * 10 की पावर - 24 ग्राम है
द्रव की द्वैत प्रकृति इलेक्ट्रॉन को साधारणतया एक कण माना जाता है इसकी तरंग प्रकृति अपेक्षाकृत कम ज्ञात है लुईस डी ब्रोग्ली ने प्रस्तावित किया कि जैसे प्रकाश की प्रकृति कण और तरंग दोनों की तरह होती है ठीक वैसे ही द्रव्य की भी द्वैत प्रकृति होती है इसे प्रायोगिक रूप से आइंस्टीन ने प्रतिपादित किया
इलेक्ट्रॉनिक ऊर्जा तलों का क्वॉन्टीकरण ( Quantization of Electronic Energy Plants )
निम्नतम अवस्था - परमाणु की न्यूनतम ऊर्जा अवस्था को निम्नतम अवस्था कहते हैं
उत्तेजित अवस्था - निम्नतम अवस्था से ऊपर पहली ऊंची ऊर्जा अवस्था को जिसमे n = 2 होता है पहली उत्तेजित अवस्था कहते हैं तथा जब n = 3 होता है तो उसे दूसरी उत्तेजित अवस्था कहते हैं
उत्तेजित विभव ( Excited potential )- एक इलेक्ट्रॉन को निम्नतम अवस्था से n तल तक उठाने के लिए आवश्यक ऊर्जा की मात्रा को उत्तेजन विभव कहते हैं
आयनन विभव ( Ionization potential )- किसी भी परमाणु के बाहरी कोश से पहले एक इलेक्ट्रॉन निकालने के लिए आवश्यक ऊर्जा की मात्रा को आयनन विभव कहते हैं
पृथक्करण ऊर्जा ( Separation Energy ) - किसी परमाण्विक बंधन को तोड़ने के लिए आवश्यक ऊर्जा को पृथक्करण ऊर्जा कहते हैं
क्वांटम संख्याएं ( Quantum Numbers ) - परमाणु के प्रत्येक इलेक्ट्रॉन की स्थिति और उसकी ऊर्जा ज्ञात करने के लिए चारो क्वांटम संख्याओं की आवश्यकता होती है
- मुख्य क्वांटम संख्या ( Principal Quantum Number )
- दिगअंशी क्वांटम संख्या ( Azimuthal quantum number )
- चुंबकीय क्वांटम संख्या ( Magnetic quantum number )
- चक्रण क्वांटम संख्या ( Spin quantum number )
1. मुख्य क्वांटम संख्या ( Principal Quantum Number ) - इसे n से प्रदर्शित करते हैं यह मुख्य ऊर्जा स्तर को बताती है आवर्त सारणी में जो एस s.p.d. f के आगे लिखी संख्या होती है वही मुख्य क्वांटम संख्या होती है
2. दिगंशी क्वांटम संख्या ( Azimuthal quantum number ) - यह क्वांटम संख्या कोश की आकृति और कोष में उपस्थित उपकोष की संख्या से संबंधित है और इलेक्ट्रॉन की कक्षीय और कोणीय वेग के कारण ऊर्जा का माप है इसे l से प्रदर्शित करते हैं l का मान 0 से n - 1 तक होता है
s.p.d. f के लिए l के मान क्रमशः 0 1 2 3 होते हैं
3. चुंबकीय क्वांटम संख्या ( Magnetic quantum number )- इस का मान सदैव 2 L + 1 होता है
4. चक्रण क्वांटम संख्या ( Spin quantum number )- प्रत्येक M के लिए दो इलेक्ट्रॉन विपरीत चक्री होते हैं
Atomic structure releated questions
प्रश्न-1 = एक तत्व आवर्त सारणी के 5वें आवर्त से संबंध रखता है तथा बाहरी कक्षा में केवल 3 इलेक्ट्रॉन है तो तत्व की चारो क्वांटम संख्याएं होंगी
A) N=5 l=4 M=9 S=18
B) N=4 l=5 M=11 S=22
C) N=3 l=4 M=9 S=18
D) N=5 l=5 M=11 S=22
प्रश्न 2 = निम्नलिखित में से कौन से नियम आफबाऊ सिद्धांत से संबंधित है
A) N + l नियम
B) हुंड का अधिकतम बहुता का नियम
C) पाउली का अपवर्जन नियम
D) उपरोक्त सभी
Specially thanks to Post and Quiz makers ( With Regards )
चित्रकूट त्रिपाठी
Leave a Reply Cancel
- बीकानेर का राठौड वंश महत्वपूर्ण प्रश्नोत्तरी 3 | राजस्थान इतिहास
- राजस्थान के लोकनृत्य से सम्बंधित प्रश्नोत्तरी
- राजस्थान के मेले और त्योहार से सम्बंधित प्रश्नोत्तरी
- October 2023 Current Affairs MCQ Test 2 | India and World
- Current Affairs October 2023 MCQ Practice Test 1
- उपसर्ग हिंदी व्याकरण महत्वपूर्ण प्रश्नोत्तरी
- Current Affairs September Free Online Test 7
- September Current Affairs Questions Mock Test 8



0 Comments